端粒是真核細胞線性染色體的末端結構,在細胞複制過程中起保護作用,避免DNA受到損傷,并且像帽子一樣有效防止染色體間末端重組、融合和染色體退化。
在細胞有絲分裂的過程中,端粒會随着分裂次數的增加逐漸縮短,當端粒縮短到一定程度時便無法繼續維持染色體的穩定,從而導緻細胞功能障礙直至死亡。因此端粒縮短也被認爲是衰老的标志,而端粒酶可以防止端粒縮短。
與人類一樣,斑馬魚腸道是端粒縮短速度最快的器官之一,在正常衰老的斑馬魚中和會導緻過早衰老的端粒酶突變體的斑馬魚中會引發早期組織功能障礙。然而,端粒依賴的單個器官(腸道)衰老是否會導緻全身衰老目前尚不清楚。
2023年5月4日,來自法國尼斯癌症與衰老研究所的Miguel Godinho Ferreira教授團隊在Nature Aging雜志發表題爲”Gut-specific telomerase expression counteracts systemic aging in telomerase-deficient zebrafish“的文章。
該研究發現腸道中組織特異性端粒酶表達可防止端粒縮短并挽救tert -/-介導的過早衰老,并且可以延長tert-/-斑馬魚40%的壽命,同時改善自然衰老。

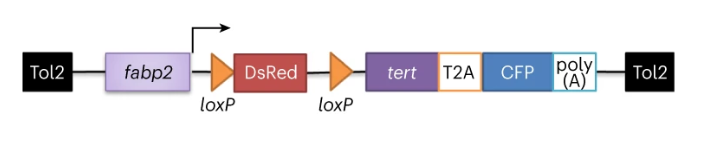
爲了研究端粒依賴性腸道衰老如何影響生物體,研究人員構造了一個斑馬魚轉基因品系,該品系包含 Cre 誘導型斑馬魚tert轉基因,由tert +/-遺傳背景中的腸細胞特異性fabp2啓動子驅動。
爲了測試tert轉基因的表達是否可以防止端粒縮短,研究人員對 9 個月大的斑馬魚腸道樣本進行了端粒限制性片段 (TRF) 分析,結果發現與對照組相比,tert敲除組血細胞的端粒長度顯著減少。盡管由fabp2啓動子驅動的tert回補 DNA (cDNA) 的表達并未将端粒長度恢複到 WT 水平,但tert轉基因的誘導也顯著延長了tert敲除組斑馬魚端粒長度。
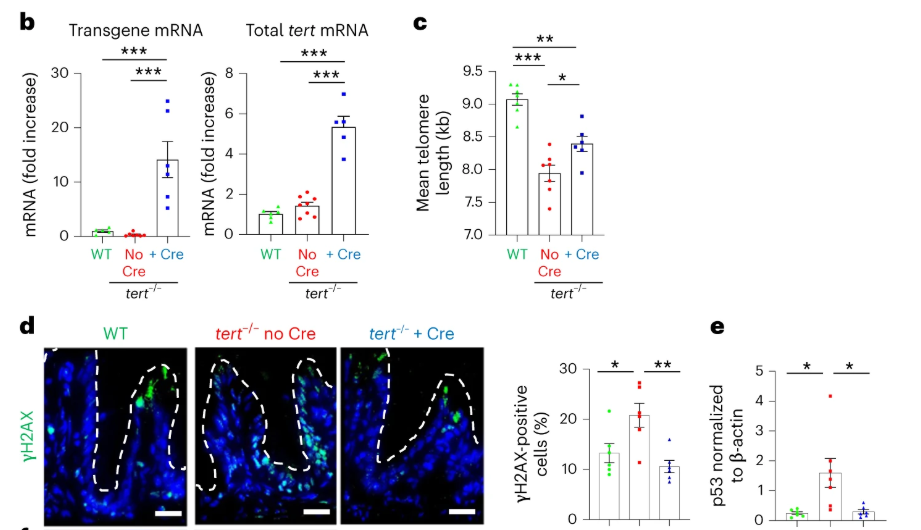
随後通過轉錄組學和代謝組學分析,确定了端粒酶表達可以挽救tert敲除斑馬魚的全身衰老症狀。具體來說,端粒酶表達可以改善腸道菌群失調、全身組織退化以及造血系統衰老等。
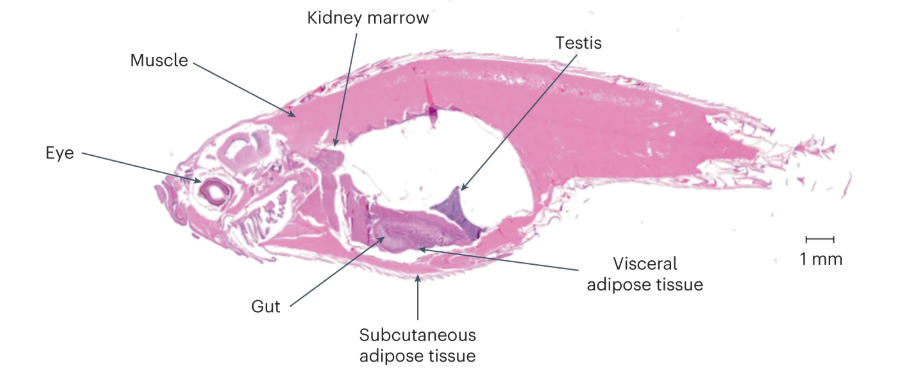
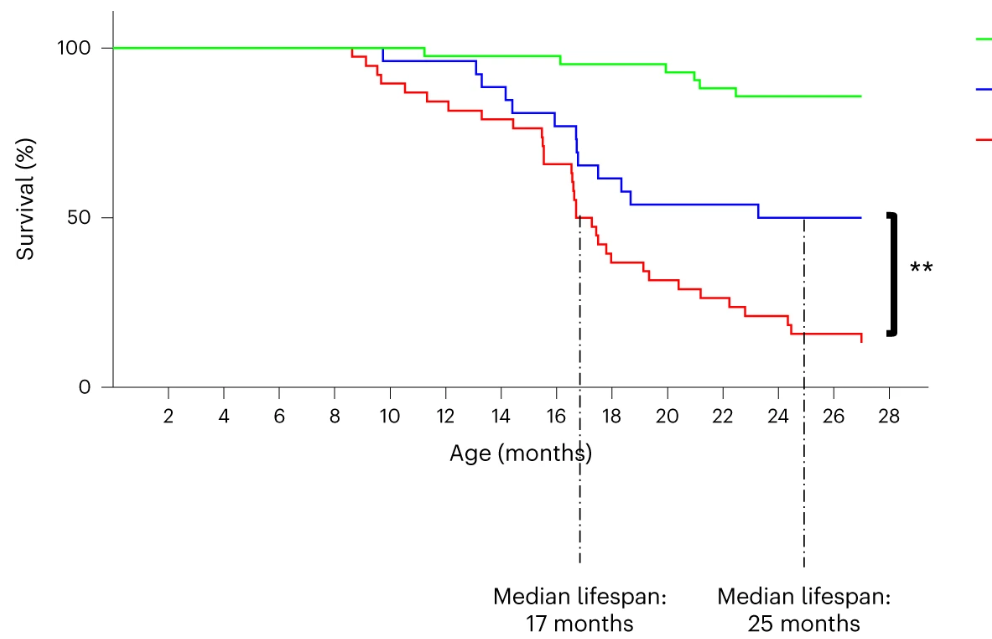
接下來研究人員測試了腸道中端粒酶的表達是否會影響斑馬魚的壽命 ,發現 tert 敲除組斑馬魚的端粒縮短,且平均壽命縮短至12-18個月,而對照組斑馬魚的平均壽命超過 42 個月。
值得注意的是,延緩腸道衰老可以将tert 敲除組斑馬魚的平均壽命延長約 40%。 然而,腸道中的端粒酶表達不足以将預期壽命完全延長到健康對照水平,這表明其他器官中的端粒縮短可能在後期也受到限制。
總而言之,該研究證明了tert 敲除斑馬魚腸道特異性端粒酶的表達可延緩腸道衰老,進而改善整個生物體的健康狀況,包括改善腸道微生物群失調和延緩多個器官的衰老。因此,腸道端粒依賴性衰老控制着整個生物體的衰老。
參考文獻:https://www.nature.com/articles/s43587-023-00401-5